İçerik
- Asıl fark
- Karşılaştırma Tablosu
- İyonik Bileşikler nedir?
- Moleküler Bileşikler nelerdir?
- İyonik Bileşikler - Moleküler Bileşikler
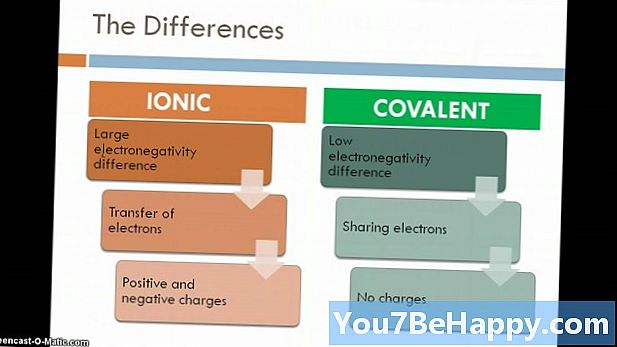
Asıl fark
Bileşik, iki veya daha fazla element belirli oranlarda bir kimyasal bağ yoluyla bir araya geldiğinde oluşan bir madde olarak kabul edilir. İyonik bileşik, metaller ile metal olmayanlar arasındaki elektrostatik çekim kuvvetinden dolayı oluşan bileşiktir. Genellikle, iyonik bileşikler satılan kristal halinde görünürler. Ayrıca, İyonik bileşikler iyi elektrik iletkenleridir ve yüksek erime ve kaynama noktalarına sahiptirler. Öte yandan, iki metal dışı arasındaki elektronların paylaşılması nedeniyle Moleküler Bileşikler oluşur. İyonik bileşiğe göre, bunlar düşük elektrik iletkenleridir ve düşük erime ve kaynama noktasına sahiptirler.
Karşılaştırma Tablosu
| İyonik bileşikler | Moleküler Bileşikler | |
| formasyon | İyonik bileşikler, metaller ile metal olmayanlar arasındaki elektrostatik çekim kuvveti nedeniyle oluşur. | Moleküler Bileşikler, metal olmayan iki metal arasındaki elektron paylaşımından dolayı oluşur. |
| grup | İyonik Bileşikler metal ile zihinsel olmayanlar arasında oluşur. | Moleküler Bileşikler, iki metalik olmayan kimyasal olarak birleştiğinde oluşur. |
| bağ | İyonik Bileşik, İyonik bağ olarak bilinen elektrostatik çekim kuvveti nedeniyle oluşur. | Moleküler Bileşikler, elemanlar arasındaki kovalent bağ nedeniyle oluşur. |
| Erime ve Kaynama Noktası | Yüksek | Düşük |
| Durum | İyonik Bileşikler, kristalli görünüm oluşturan her zaman katı haldedir. | Moleküler Bileşikler oda sıcaklığında herhangi bir durumda, katı, sıvı veya gaz halinde olabilir. |
| Elektrik Şefi | İyi | Kötü |
İyonik Bileşikler nedir?
Bu bileşikler, metaller ile metal olmayanlar arasındaki elektrostatik çekim kuvveti nedeniyle oluşur. Daha basit bir ifadeyle, bunun içindeki kuvvet (iyonik bağ) bir bileşik oluşturmak için birlikte pozitif ve negatif olarak yüklü tepki verir. Genellikle, iyonik bileşikler satılan kristal halde görünür ve yüksek erime ve kaynama noktalarına sahip iyi elektrik iletkenleridir. İyonik Bileşikler metaller ile metal olmayanlar arasında oluşur ve bir çeşit parlak görünüme sahiptir.
Örnek: Sofra Tuzu (NaCl) en yaygın İyonik Bileşik örneğidir. Bu oluşumda, Sodyum (NA) metaldir, oysa Klor (Cl) metal değildir, ikisi de arasındaki elektrostatik çekim kuvveti nedeniyle ikisi bir arada tutulur.
Moleküler Bileşikler nelerdir?
Metal olmayan metaller arasında elektron paylaşımı nedeniyle oluşan bileşikler Moleküler Bileşik olarak bilinir. Burada reaksiyona giren elementler kovalent bağlanma nedeniyle bir arada tutulur ve bu nedenle bu bileşiklere genellikle Kovalent Bileşikler denir.İyonik bileşiğe göre, bunlar düşük elektrik iletkenleridir ve düşük erime ve kaynama noktasına sahiptirler.
Örnek: Ozonda (O3), Oksijen, Ozon oluşturmak için elektronların paylaşımı ile birleşir.
İyonik Bileşikler - Moleküler Bileşikler
- İyonik bileşikler, metaller ile metal olmayanlar arasındaki elektrostatik çekim kuvveti nedeniyle oluşturulurken, Moleküler Bileşikler, iki metal olmayan metal arasında elektronların paylaşılması nedeniyle oluşur.
- Moleküler Bileşikler, iki metal içermeyen kimyasal olarak birleştiğinde, diğer yandan, İyonik Bileşikler metal ile zihinsel olmayan arasında oluşturulmaktadır.
- Moleküler Bileşikler, elementler arasındaki kovalent bağ nedeniyle oluşturulurken İyonik Bileşik, İyonik bağ olarak bilinen elektrostatik çekim kuvveti nedeniyle oluşturulur.
- Moleküler Bileşikler, İyonik Bileşikler ile karşılaştırıldığında düşük erime ve kaynama noktasına sahiptir.
- Moleküler Bileşikler, oda sıcaklığında herhangi bir durumda, katı, sıvı veya gaz halinde olabilirken, İyonik Bileşikler kristalli bir görünüm oluşturarak her zaman katı haldedir.
- Moleküler Bileşikler elektrik iletkenliği zayıf, İyonik Bileşikler ise elektrik iletkenliği iyidir.


